











一、大腸菌群簡介
大腸菌群是指一群37℃、24h發酵乳糖、產酸產氣的需氧和兼性厭氧革蘭氏陰性無芽胞杆菌。主要由腸杆菌科中四個屬內的一些細菌所組成,即埃希氏菌屬、檸檬酸杆菌屬、克雷伯氏菌屬以及腸杆菌屬。該菌主要來源於人畜糞便,故以此作為糞便汙染指標來評價食品的衛生質量,推斷食品中有否汙染腸道致病菌的可能。
二、參考標準
《GB4789.3-2016 食品安全國家標準 食品微生物學檢驗 大腸菌群計數》
三、檢驗方法及原理
1.MPN法
MPN法是統計學和微生物學結合的一種定量檢測法。待測樣品經係列稀釋並培養後,根據其未生長的最低稀釋度與生長的最高稀釋度,應用統計學概率論推算出待測樣品中大腸菌群的最大可能數。MPN法適用於大腸菌群含量較低的食品中大腸菌群的計數。
2.平板計數法
大腸菌群在固體培養基中發酵乳糖產酸,在指示劑的作用下形成可計數的紅色或紫色,帶有或不帶有沉澱環的菌落。平板計數法適用於大腸菌群含量較高的食品中大腸菌群的計數。
四、檢驗流程
(一)MPN法
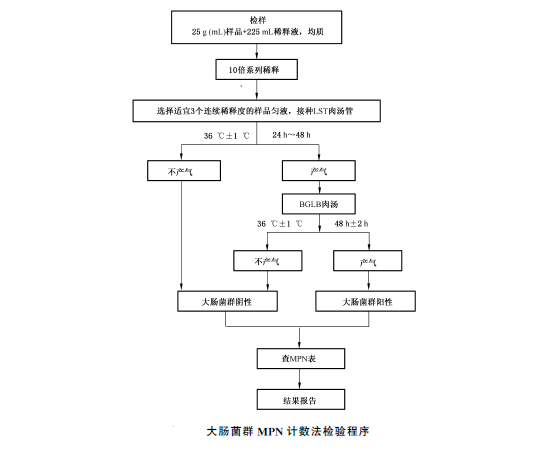
1、初發酵試驗
選擇3個適宜的連續稀釋度的樣品勻液(液體樣品可以選擇原液),每個稀釋度接種3管月桂基硫酸鹽胰蛋白腖(LST)肉湯,每管接種1mL(如接種量超過1mL,則用雙料LST肉湯),36℃±1℃培養24h±2h,觀察倒管內是否有氣泡產生,24h±2h產氣者進行複發酵試驗(證實試驗),如未產氣則繼續培養至48h±2h,產氣者進行複發酵試驗。未產氣者為大腸菌群陰性。
檢驗原理:胰蛋白腖在培養基中作為營養物質提供菌體細胞生長所需要的氮源、維生素、氨基酸及生長因子等;乳糖提供菌體細胞生長所需要的碳源;氯化鈉維持體係滲透壓平衡;磷酸鹽為菌體生長提供相對穩定的酸堿緩衝體係;月桂基硫酸鈉抑製非大腸菌群類細菌的生長。
培養基用法:稱取本品35.6克,加熱溶解於1000mL蒸餾水中,分裝到有倒立發酵管的20mm×150mm試管中,每管10mL,121℃高壓滅菌15分鍾,備用。質控菌株接種到LST肉湯管中,培養結果如圖1所示。
注意事項:液體樣品可以選擇原液;若是接種量需要超過1mL,則用雙料LST肉湯。

圖1 月桂基硫酸鹽胰蛋白腖(LST)肉湯微生物質控結果
2、複發酵試驗
用接種環從產氣的LST肉湯管中分別取培養物1環,移種於煌綠乳糖膽鹽肉湯(BGLB)管中,36℃±1℃培養48h±2h,觀察產氣情況。產氣者,計為大腸菌群陽性管。
檢驗原理:蛋白腖提供碳氮源;乳糖是可發酵的糖類;牛膽粉和煌綠抑製非腸杆菌科細菌。
培養基用法:稱取本品40.0g,加熱攪拌溶解於1000mL蒸餾水中,分裝到有倒立發酵管的20mm×150mm試管,每管10mL,121℃高壓滅菌15分鍾,備用。質控菌株接種到BGLB肉湯管中,培養結果如圖2所示。

圖2 BGLB肉湯微生物質控結果
3、結果判定
根據證實為大腸菌群的陽性管數,查大腸菌群最可能數(MPN)檢索表,報告每g (mL)大腸菌群的MPN值。
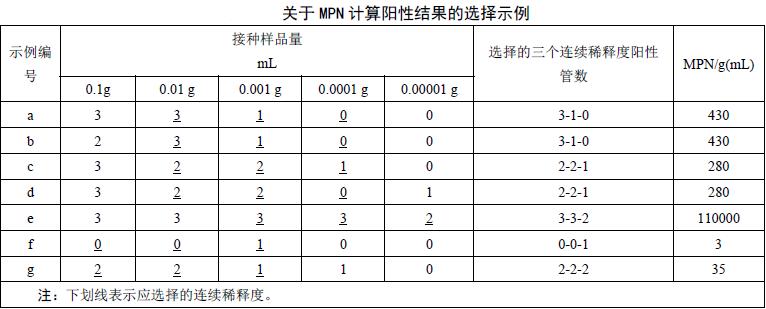
確定最適的三個連續稀釋度方法,在10-1~10-5五個連續稀釋度中確定最適的三個連續稀釋度方法如下:
a)有一個以上的稀釋度3管均為陽性。選擇三管都是陽性結果的最高稀釋度及其相連的兩個更高稀釋度(見示例a、b,表中帶下劃線的數字對應的接種樣品量為最終選取的最適稀釋度,下同);
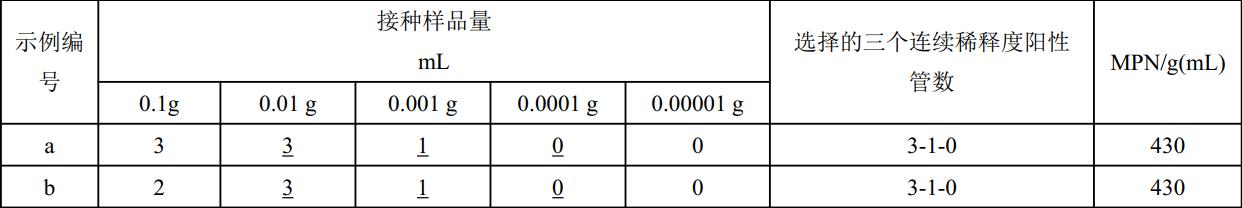
b)在未選擇的較高稀釋度中還有陽性結果時,則順次下移到下一個更高三個連續稀釋度(見示例c);
![]()
如果中間有某個稀釋度沒有陽性結果,但更高稀釋度有陽性結果,則將此陽性結果加到前一稀釋度,進而確定三個連續稀釋度(見示例d);
![]()
如果不能按照這個原則找到三個合適的稀釋度,則選擇前一個較低的稀釋度(見表示例e);
![]()
c)沒有任何一個稀釋度3管均為陽性。如果沒有一個稀釋度的3管均為陽性,則選擇三個最低稀釋度(見示例f);
![]()
如果在更高的沒有被選擇的稀釋度還有陽性結果,將此陽性結果加到選擇的最高稀釋度,進而確定三個連續稀釋度(見示例g)。
![]()
每g(mL)檢樣中大腸菌群最可能數(MPN)的檢索表:

舉例說明:若糞大腸菌群的陽性管數的示例為3-3-2-0-1,則選擇的稀釋度為3-2-1,根據MPN檢索表所得MPN數值為1500。
(二)平板計數法
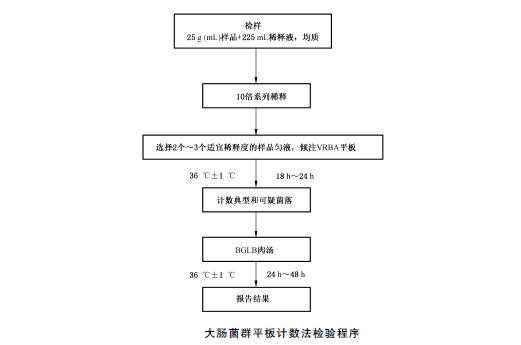
1、平板計數
選取2個~3個適宜的連續稀釋度,每個稀釋度接種2個無菌平皿,每皿1mL。同時取1mL生理鹽水加入無菌平皿作空白對照。將15mL~20mL融化並恒溫至46℃的結晶紫中性紅膽鹽瓊脂(VRBA)約傾注於每個平皿中。小心旋轉平皿,將培養基與樣液充分混勻,待瓊脂凝固後,再加3mL~4mLVRBA覆蓋平板表層。翻轉平板,置於36℃±1℃培養18h~24h。
檢驗原理:蛋白腖和酵母浸粉提供碳氮源、維生素、生長因子和輔酶等其他營養物質;氯化鈉維持均衡的滲透;乳糖為可發酵碳水化合物,可作為一種能量來源;3 號膽鹽和結晶紫可抑製革蘭氏陽性菌的生長;中性紅為指示劑;瓊脂是培養基的凝固劑。大腸菌群可以發酵乳糖產酸,在中性紅指示劑作用下形成紫紅色菌落。
培養基用法:稱取本品41.5g,加熱溶解於1000mL蒸餾水中,煮沸不要超過2分鍾。
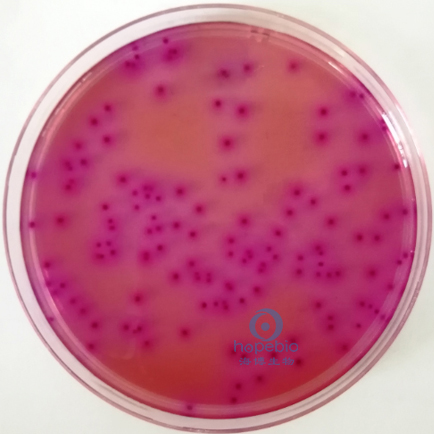
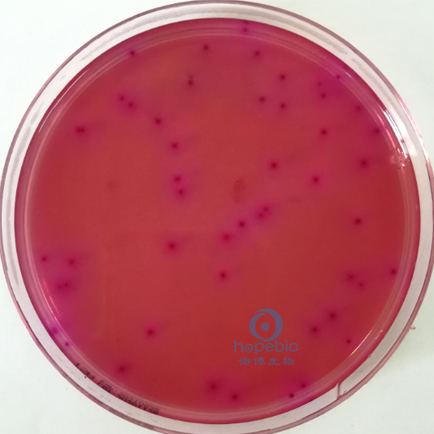
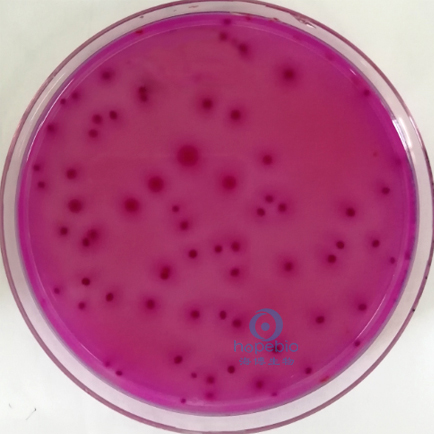
選取菌落數在15CFU~150CFU之間的平板,分別計數平板上出現的典型和可疑大腸菌群菌落(如菌落直徑較典型菌落小)。典型菌落為紫紅色,菌落周圍有紅色的膽鹽沉澱環,菌落直徑為0.5mm或更大,最低稀釋度平板低於15CFU的記錄具體菌落數。質控菌株接種到VRBA培養基中,培養結果如圖3所示。
 |
 |
|||
| 大腸埃希氏菌 |
弗氏檸檬酸杆菌 |
|
|
|
 |
 |
|||
| 陰溝腸杆菌 | 鼠傷寒沙門氏菌 |
注意事項:選取菌落數在15CFU~150CFU之間的平板,菌落形態應為為紫紅色,菌落周圍有紅色的膽鹽沉澱環,菌落直徑為0.5mm或更大,最低稀釋度平板低於15CFU的記錄具體菌落數。
2、證實試驗
從VRBA平板上挑取10個不同類型的典型和可疑菌落,少於10個菌落的挑取全部典型和可疑菌落。分別移種於BGLB肉湯管內,36℃±1℃培養24h~48h,觀察產氣情況。凡BGLB肉湯管產氣,即可報告為大腸菌群陽性。質控菌株接種到BGLB肉湯管中,培養結果如圖4所示。

圖4
3、平板計數法計數結果
經最後證實為大腸菌群陽性的試管比例乘以計數的平板菌落數,再乘以稀釋倍數,即為每g(mL)樣品中大腸菌群數。若所有稀釋度(包括液體樣品原液)平板均無菌落生長,則以小於1乘以最低稀釋倍數計算。
舉例說明:10-4樣品稀釋液1mL,在VRBA平板上有100個典型和可疑菌落,挑取其中10個接種BGLB肉湯管,證實有6個陽性管,則該樣品的大腸菌群數為:100×6/10×104/g(mL)=6.0×105CFU/g(mL)。
注:本文屬betway必威西汉姆联生物原創,未經允許不得轉載。
下一篇:糞大腸菌群計數標準解析

