











第一節 藥品微生物檢驗結果的影響因素
微生物的生長受很多因素的影響,特別是藥品中汙染的微生物尤為如此。藥品微生物檢驗是檢測藥品中具有繁殖能力的活細胞,這些活的微生物在藥品中處於不穩定的狀態,它的檢出與否受很多因素的影響,主要影響因素有如下幾點:
一、 供試品組分
由於供試品本身的特性,可能含有具有抑菌作用的組分成分,如抗生素中藥中的黃蓮、牛黃、冰片等。另外,很多供試品中加入的抑菌劑或防腐劑用於防止供試品中的微生物再汙染和再生殖,以及增溶劑、乳化劑、抗氧劑等其他輔料,這些組分在一定濃度下對 微生物具有抑製作用,並可能對 藥品中汙染的微生物造成不同程度的損傷。供試品中汙染的微生物在這些物質的影響下有可能檢不出,這時,它們雖然被 抑製甚至受到損傷,但並未死亡,在一定條件在塔門還可以穩定地存活一段時間,當微生物生存環境改變時,如抑菌成分消除或濃度降低時,這些微生物便可以複蘇並繁殖,患者使用後同樣可危及人體健康。對於這些藥品,如按常規方法進行微生物檢驗,往往顯示假陰性結果。
除此之外,在藥品微生物檢驗中,由於原料來源不同,特別是中藥製劑,或者生產工藝的差別,使用的輔料不同等原因,使不同廠家生產的同一產品,甚至是同一廠家生產的同一產品不同批次的藥品往往對同一中微生物的生長也有 不同程度的影響。
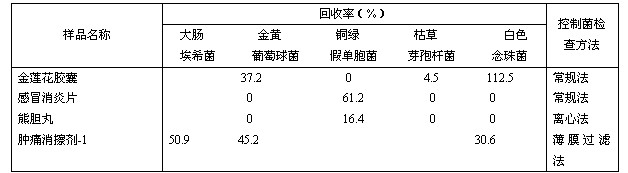
從理論上講,許多藥品含有影響微生物生長的物質,許多試驗也表明了這一點,表12-1列出了已知試驗菌的菌數在不同藥品中的回收率,有的藥品幾乎對所有試驗菌均有很強的抑製或殺死作用。因此,供試品的組分及其濃度直接影響供試品中汙染微生物的檢查結果準確與否。
表12-1 回收率小於70%樣品的各試驗菌回收試驗結果
一、 微生物的多樣性及複雜性
自然界中微生物的種類和生存形式是多種多樣的,藥品的種類繁多,劑型多樣,其汙染的微生物也是多樣而複雜的,即使是同一產品的生產區域,所汙染的微生物種類也不盡相同;同一產品因存放的時間和條件不同,其中汙染微生物存在的形式可能改變(菌體或孢子等狀態)。不同類型的微生物及不同的存活狀態對環境的抗性是不同的,采用同一檢查方法未必是適宜的。
藥品中汙染的微生物,特別是生產前期汙染的,受到原料處理、加工、加熱等過程的影響,均可能受到一定程度的損傷。這些受損但尚存活的微生物可能遭受外界環境的抑製,隻有在適宜的條件下使其修複或從抑製狀態中複蘇後,才能正常生長。否則,這些微生物就很難檢出。
二、 藥品微生物的檢查方法
檢查方法包括供試液製備方法和微生物檢測方法,它是保證檢驗結果準確可靠的最重要前提。
微生物檢測時,首先進行供試液的製備,不同特性的供試品,應采用不同的供試液製備方法,如水溶性供試品直接加稀釋劑製備即可;不溶水的固體供試品采用勻漿或加混懸劑製成均勻的混懸液;非水溶性油劑或軟膏劑,因其與水難溶,使其中汙染的微生物難與培養基接觸或因缺氧而無法生長,需采用乳化劑使成均勻分散的乳濁液;有抑菌成分的供試品客加入消除抑菌成分的中和劑;離心沉澱及薄膜過濾消除抑菌成分的方法等,這些物理或化學的供試液製備方法在進行過程或多或少影響著供試品中微生物的回收。
同一份供試液采用不同的微生物檢測方法,如常規法、培養基稀釋法、薄膜過濾法、MPN法等,其檢測的結果可不同,因為其中所含的供試品濃度不同,特別是有抑菌作用的供試品。
三、 檢驗條件
藥品中汙染的微生物的檢驗是基於微生物在培養基中的生長情況進行結果判斷。因此,培養基質量、PH、培養溫度、培養時間及供氧情況等均影響微生物的生長,導致了檢驗結果的差異。
除此之外,試驗人員操作的誤差,不同實驗室的誤差等原因,均可影響微生物的檢出結果。
第一節 藥品微生物檢驗方法驗證的意義及概況
一、 藥品微生物檢驗方法驗證的意義
正因為藥品中汙染的微生物檢查結果受很多很多結果的影響,加上生物本身的誤差就很大。這些將直接影響樣品中微生物的回收(見表12-2),從表12-2看,試驗樣品中,試驗菌的回收率小於10%、50%、70%及80%的樣品分別占25.3%、33.9%、35.5%及40.3%。試驗結果表明了按現版的藥典方法測定藥品中汙染的微生物,對有些樣品來說,其結果不能真實反映樣品的汙染狀況。在這種情況下,該方法也及時去其原有的意義。另外,任何檢查法均有它的局限性,同一種供試品的微生物限度檢查因采用的檢查方法和檢查條件不同,導致了不同的菌數測定結果,它將直接影響著檢驗結果的判定(見表12-3)。因此,在進行藥品中微生物檢驗中,隻有在各檢測條件均適宜時,即在該檢驗條件下的樣品濃度不足以抑製汙染微生物的生長,使供試瓶中汙染的微生物得以真實的反映,從而保證結果的哦科學性準確性。因此,其他分析方法一樣,藥品的無菌檢查和微生物限度檢查也應證明所采用的方法是適宜的。確認所采用的方法適合於樣品的微生物汙染的檢查,方可使用。
表12-2 試驗菌在樣品中回收情況
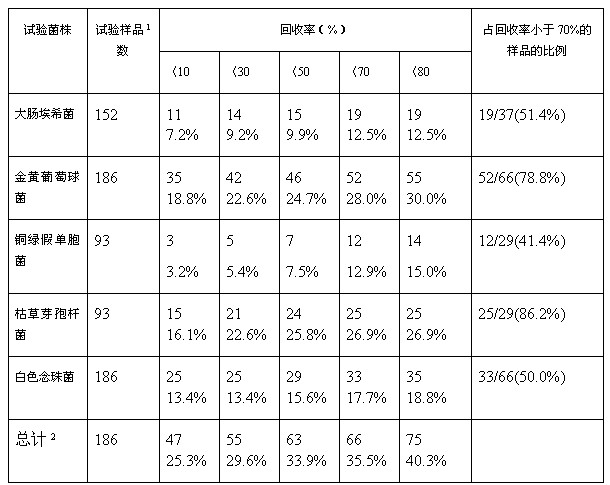
注1:有的樣品隻測定部分試驗菌株。
注2:指各樣品至少有一株的回收率規定。
表12-3 同一樣品不同檢測方法的微生物回收率情況
二、國外藥典藥品微生物檢驗方法驗證的概況
在美國藥典、歐洲藥典、日本藥局對無菌檢查法和微生物限度檢查法協調之前,USP、BP、EP、JP對無菌檢查法和微生物限度檢查方法的驗證要求提出要求。USP24版規定了在進行無菌檢查和微生物限度檢查時,應如何進行藥物中微生物回收的驗證試驗,同時要求在檢查時,應消除供試品的抑菌活性,以保證試驗結果的可信性;USP24版的無菌檢查法中還規定了無菌檢車時應進行樣品的抑細菌、抑真菌試驗。BP1993版無菌檢查法中雖未單列抑細菌、抑真菌試驗,但在培養基促生長試驗中含有加供試品組以觀察供試品是否含有抑菌活性,事實上是培養基促生長試驗與抑細菌、抑真菌試驗同時進行;BP1998版就比較詳細的規定應如何及何時進行藥品無菌檢驗法的驗證,在微生物限度檢查法中也同時要求應進行培養基質量和檢查方法的確認。
下一篇:微生物毒素

